
"مشاهده" پروتئین سمی هانتینگتین در افراد مبتلا به HD
ابزارهای جدید به ما اجازه می دهند توده های پروتئین سمی هانتینگتین را که در طول زمان در مغز افراد مبتلا تجمع می یابد، ببینیم. ردیابی این توده ها ممکن است به ما کمک کند تا درک بهتری از چگونگی پیشرف HD،کند شدن یا توقف بیماری در طول درمان،داشته باشیم.
دانشمندان ابزاری ابداع کردهاند که به ما امکان میدهد تودههای سمی پروتئین هانتینگتین را با استفاده از اسکنرهای ویژه «مشاهده» کنیم. افراد مبتلا به بیماری هانتینگتون (HD) فرم سمی پروتئین هانتینگتین را می سازند که در سلول های بدن آنها توده هایی ایجاد می کند که در طول پیشرفت HD تجمع می یابد. ردیابی اینکه چگونه این تودهها در طول زمان در افراد مبتلا به HD شکل میگیرند، یا اینکه وقتی افراد مبتلا به HD از درمانهای مختلف استفاده میکنند، چگونه تغییر میکنند، میتواند به ما در درک بهتر پیشرفت HD و اینکه کدام داروها بیشتر به بیماران کمک میکنند، یاری برساند.
این توده های پروتئینی چیست؟
همه ما 2 نسخه از ژن هانتینگتین داریم، اما برای افرادی که بیماری هانتینگتون (HD) دارند، یکی از نسخه های آنها نوعی جهش به نام تکرار افزایش یافته دارد. این جهش در دورهّای تکراری در بخشی از کد DNA ژن هانتینگتین رخ می دهد که حروف “C"، "A” و “G” بارها و بارها تکرار می شوند. اگر HD ندارید، کمتر از 35 تکرار CAG در ژن هانتینگتین خود دارید، اما برای افراد مبتلا به HD، جهش به این معنی است که آنها بیش از 35 تکرار CAG در یکی از ژن هانتینگتین خود دارند.

ژن هانتینگتین دستوری است که سلول های ما برای ساختن پروتئین هانتینگتین استفاده می کنند، بنابراین اگر کد DNA این دستور تغییر کند، پروتئینی که بدن ما می سازد نیز تغییر خواهد کرد. پروتئین ها از زنجیرههای بلندی از مواد شیمیایی به نام اسیدهای آمینه ساخته می شوند که از دستورالعمل های مندرج در DNA ما پیروی می کنند. حروف DNA “CAG” دستوری برای ساخت اسید آمینه گلوتامین است. این بدان معنی است که اگر تعداد تکرار CAG بزرگتر شود، پروتئین هانتینگتین گلوتامین های تکرار شونده بیشتری خواهد داشت. مولکول های پروتئین هانتینگتین با گلوتامین های زیاد نمی توانند به درستی ساخته شوند، بنابراین می توانند توده های سمی ایجاد کنند.
ما مدت زیادی است که در مورد این توده ها می دانیم و وقتی زیر میکروسکوپ نگاه می کنیم در مغز افراد مبتلا به HD دیده می شود. با این حال، ردیابی این تودهها در بیماران زنده چالش برانگیز بوده و بیشتر دانش ما از آنها از نگاه کردن به آنها در نمونههای مغز پس از مرگ از مدلهای حیوانی HD یا بیمارانی حاصل میشود که با مهربانی مغز خود را به تحقیق اهدا کردهاند.
چرا می خواهیم به این توده های مزاحم نگاه کنیم؟
دانشمندان از آزمایشگاههای متعددی در انگلستان، آلمان، ایتالیا، سوئد و ایالات متحده، ابزارهای مولکولی توسعه دادهاند که اکنون به ما امکان میدهند این تودهها را در حیوانات زنده “مشاهده” کنیم و امیدوارم به زودی، در بیماران HD نیز بتوانیم از این ابزارها استفاده کنیم. این ابزارها به تودههای پروتئین هانتینگتین متصل میشوند و دارای تزئینات شیمیایی به نام رادیوبرچسب هستند که به معنی این است که وقتی با استفاده از اسکن PET (توموگرافی گسیل پوزیترون) مورد بررسی قرار گیرند، روشن میشوند.
این نوع ابزارهای مولکولی به عنوان ردیابهای PET شناخته میشوند و در بسیاری از تنظیمات پزشکی و تشخیصی مختلف استفاده میشوند تا به پزشکان و محققان امکان تصویربرداری از بخشهای خاص بدن شما را بدهند. بسته به اینکه چه قسمتی از بدن شما قرار است بررسی شود ، انواع مختلفی از ردیاب ها را می توان بلع، تزریق یا استنشاق کرد. پس از ورود ردیاب PET به بدن بیمار، او مورد اسکن قرار میگیرد و بخشی از بدن که در آن هدف ردیاب PET وجود دارد، روشن میشود زیرا ردیاب کمی رادیواکتیو است. ابزارهای مشابهی برای مطالعه سایر بیماریها مانند ترکیب B پیتسبورگ ساخته شدهاند که برای مشاهده تودههای مشابه در افراد مبتلا به آلزایمر استفاده میشود.
ساخت ردیابهای PET که به محققان امکان میدهد تودههای سمی پروتئین هانتینگتین را ببینند، این ایده به دلایل متعدد جذاب است. اولاً،اسکن PET را می توان در چندین مقطع زمانی در طول زندگی بیماران روی آنها انجام داد تا بتوانیم نحوه تجمع توده ها را در طول زمان پیشرفت HD ردیابی کنیم. بسیاری از روشهای کنونی ما برای مشاهده توده هانتینگتین در مغز بیماران فعلی فقط در انتهای بیماری در نمونههای بافتی پس از مرگ قابل انجام هستند.
ثانیاً، اسکن PET روشی غیرتهاجمی است و به ما امکان میدهد به مغز نگاهی اساسی بیندازیم، در حالی که روشهای دیگری مانند اندازهگیری پروتئین هانتینگتین در مایع مغزی نخاعی تنها مقطعی از آنچه که فکر میکنیم در مغز اتفاق میافتد را ارائه میدهند. سوماً، تودهها از نوع سمی پروتئین هانتینگتین تشکیل میشوند، بنابراین اسکنهای PET به محققان امکان میدهد به طور خاص تغییراتی را در این شکل جهش یافته از هانتینگتین اندازهگیری کنند. این با بسیاری از روش هایی که ما هانتینگتین را در مایع نخاعی یا خون اندازه گیری و تجزیه و تحلیل می کنیم که تمام اشکال مختلف هانتینگتین، از جمله پروتئین هانتینگتین سالم را اندازه گیری می کند، متفاوت است.
توسعه اولین لیگاند PET Huntingtin
آگوست گذشته، نسخه اولیه این ابزار به نام CHDI-180R منتشر شد – اولین باری که یک ردیاب PET برای پروتئین هانتینگتین ساخته شد! تیمی به رهبری سلیا دومینگوئز در بنیاد CHDI نشان دادند که مولکول ابزار CHDI-180R میتواند بسیار محکم به تودههای پروتئین سمی هانتینگتین در یک لوله آزمایش متصل شود. آنها همچنین از CHDI-180R برای نشان دادن محل تودههای هانتینگتین سمی در نمونههای مغزی مدلهای موش HD استفاده کردند.
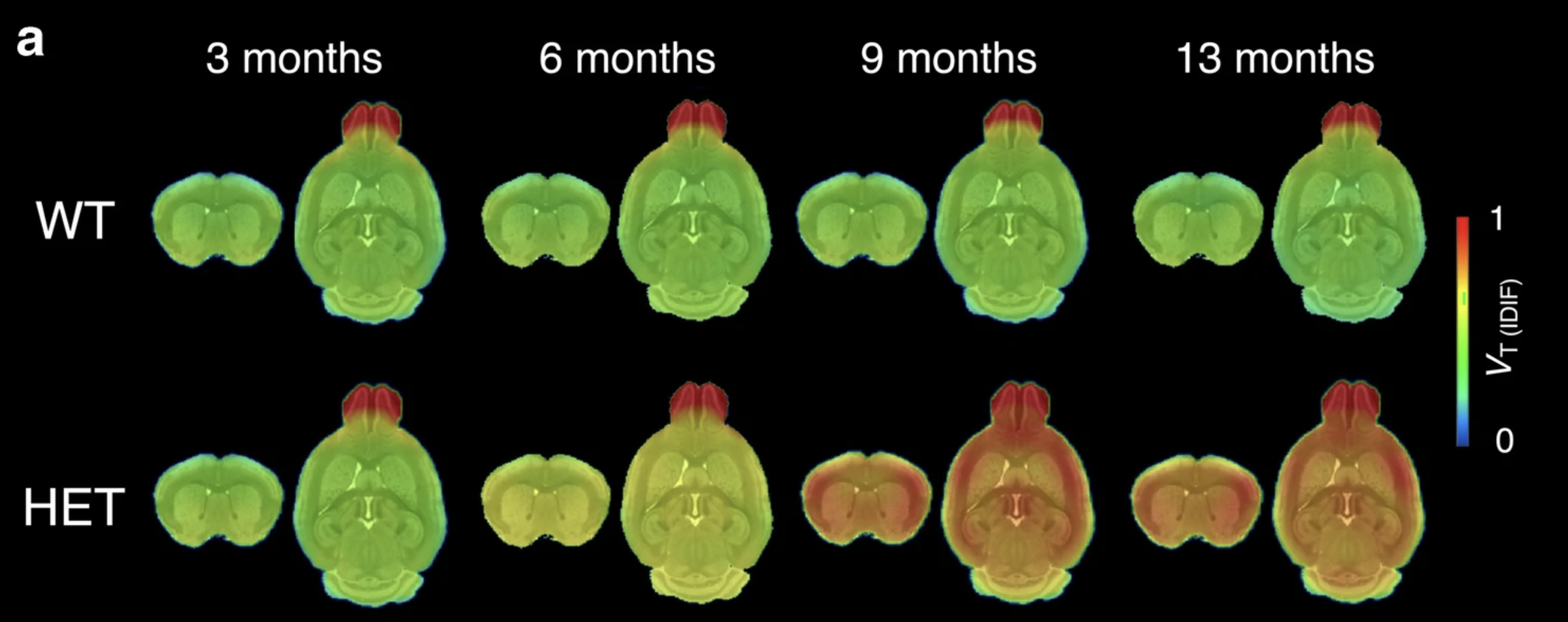
Image credit: Bertoglio et al (2021) Eur J Nucl Med Mol Imaging
در مغز موشهای دارای جهش HD، تودههایی از پروتئین سمی هانتینگتین را میتوان در بسیاری از نواحی مختلف مغز که تحت تأثیر HD هستند، مشاهده کرد، در حالی که در موشهای بدون جهش HD، این تودهها قابل مشاهده نبودند، حتی اگر به آنها نیز مولکول ابزار CHDI-180R تزریق شده بود. در نهایت، دانشمندان نشان دادند که CHDI-180R به خوبی در سراسر مغز پخش میشود و همچنین در میمونها و موشها بیخطر است.
تنظیم دقیق ابزارها
توسعه ردیاب PET اغلب قبل از یافتن یک ابزار بهینه نیاز به تلاشهای متعدد دارد، بنابراین همان گروه بینالمللی از دانشمندان در حال توسعه نسخههای دیگر این ردیاب هستند تا گزینههای پشتیبان زیادی داشته باشند. نسخههای جدید و بهبود یافته این ابزار مولکولی در حال آزمایش هستند تا نحوه انتشار آنها در مغز حیوانات آزمایش شده مشخص شود.
سایر بیماریها مانند آلزایمر نیز دارای تودههای پروتئینی هستند که در سلولهای عصبی انباشته میشوند، اما اینها از پروتئینهای بالقوه سمی دیگر مانند آمیلوئید بتا ساخته شدهاند. دانشمندان همچنین بررسی می کنند که چقدر این ابزارها برای توده های پروتئین هانتینگتین که در طول زمان در بیماران HD انباشته می شوند در مقایسه با سایر توده های پروتئین بیماری مانند بیماران آلزایمر ، به طور اختصاصی عمل میکنند. تاکنون، نتایج بسیار دلگرم کننده بوده است، بنابراین دانشمندان اکنون مشتاق هستند که آزمایش ردیاب ها را در انسانها آغاز کنند.
چه اقداماتی پیش روی ماست؟
یک کارآزمایی بالینی به نام مطالعه iMagemHTT در حال انجام است که ردیاب هانتینگتین را در افراد بررسی می کند. این کارآزمایی از تصویربرداری PET/MRI برای درک اینکه لیگاند PET چگونه هانتینگتین را در مغز ردیابی میکند، استفاده خواهد کرد. قبلاً در نشست مجازی CHDI در اوایل سال جاری، برخی از دادههای اولیه دلگرمکننده از مطالعه فاز اول این ردیاب را گزارش کردیم. تاکنون، یافتهها دلگرمکننده هستند، بنابراین آنها همچنان به اضافه کردن شرکتکنندگان به مطالعه ادامه میدهند. مقدار توده هانتینگتین در مغز افراد مبتلا به HD نشانگر زیستی خوبی برای پیشرفت بیماری است. بیومارکرها اندازهگیریهای عینی هستند که دانشمندان و پزشکان میتوانند برای ردیابی پیشرفت HD انجام دهند که میتواند برای یافتن بهترین گزینههای درمانی و همچنین بررسی کیفیت عملکرد درمانها مهم باشد. این امکان وجود دارد که بیماران HD در آینده با اسکن PET و با استفاده از این نوع ابزارها تحت نظر باشند. اگر لیگاندهای PET به طور مطلوب کار کنند، میتواند در آزمایشهای آتی برای پیگیری کاهش هانتینگتین در مغز نیز مورد استفاده قرار بگیرد. با وجود مشکلاتی که در برخی از آنها وجود دارد، کاهش هانتینگتین هنوز یک استراتژی امیدوارکننده برای درمان بیماری هنتینگتون است که توسط شرکتهای Novartis، PTC Therapeutics، Wave و Uniqure که همه آنها آزمایشات بالینی در دست انجام دارند، پیگیری میشود. صرف نظر از اینکه با کاهش هانتینگتین چه اتفاقی میافتد، این ابزارهای جدید هیجانانگیز به دانشمندان این توانایی را میدهند – برای اولین بار – پروتئین جهشیافته هانتینگتین را در سراسر مغز بیماران زنده HD ردیابی کنند، که پیشرفت بزرگی است.
ما منتظر به روزرسانیهای بیشتر در این زمینه هستیم!
بیشتر بدانید
- تصویربرداری از تجمعات جهش یافته هانتینگتین: توسعه یک لیگاند PET بالقوه (open access)
- [ 11 C] CHDI-626، یک کاندید ردیاب PET برای تصویربرداری از توده های هانتینگتین جهش یافته با کاهش اتصال به پروتئین های پاتولوژیک AD است. (open access)
- ارزیابی طولانی بالینی رادیو لیگاند جدید [11C]CHDI-626 برای تصویربرداری PET از تجمعات های هانتینگتین جهش یافته در بیماری هانتینگتون (open access)
- توصیف فارماکولوژیکی از ردیابهای تصویربرداری PET هدایت شده به سمت تجمعات هانتینگتین جهش یافته (open access)
For more information about our disclosure policy see our FAQ…


