
هدف قرار دادن پیامرسان با خاموشسازی ژن RNA تکرشتهای
داروهای جدید خاموشسازی ژن ‘RNA تکرشتهای’ میتوانند برای درمان بیماری هانتینگتون ایمنتر و مؤثرتر باشند
احتیاط: ترجمه خودکار – احتمال خطا
برای انتشار اخبار تحقیقات HD و بهروزرسانیهای آزمایشی در اسرع وقت به حداکثر تعداد افراد، این مقاله به طور خودکار توسط هوش مصنوعی ترجمه شده و هنوز توسط ویراستار انسانی بررسی نشده است. در حالی که ما تلاش میکنیم اطلاعات دقیق و قابل دسترس ارائه دهیم، ترجمههای هوش مصنوعی ممکن است حاوی خطاهای دستوری، تفسیرهای نادرست یا عبارات نامفهوم باشند.برای اطلاعات موثقتر، لطفاً به نسخه اصلی انگلیسی مراجعه کنید یا بعداً برای ترجمه کاملاً ویرایششده توسط انسان دوباره مراجعه کنید. اگر متوجه مشکلات قابل توجهی شدید یا اگر زبان مادری شما این زبان است و میخواهید در بهبود ترجمههای دقیق کمک کنید، لطفاً با editors@hdbuzz.net تماس بگیرید.
پس از پیشرفتهای چشمگیر در سالهای اخیر، ما به آزمایشهای انسانی کاهش هانتینگتین یا ‘خاموشسازی ژن’ به عنوان یک درمان بالقوه برای بیماری هانتینگتون نزدیکتر میشویم. تکنیکهای جدیدتر، بهتر و ایمنتر همیشه مورد استقبال قرار میگیرند و اعلام ‘خاموشسازی RNA تکرشتهای’ هیاهوی زیادی به پا کرده است. ماجرا از چه قرار است؟
داروهای خاموشسازی ژن با دستور دادن به سلولها برای عدم تولید پروتئین هانتینگتین، عامل آسیب در بیماری هانتینگتون، عمل میکنند. آنها این کار را با مداخله در سیستمهای پروتئینسازی سلولها انجام میدهند.
دو نوع اصلی داروی خاموشسازی ژن وجود دارد: الیگونوکلئوتیدهای آنتیسنس (ASO) و تداخل RNA (RNAi). این مقاله در مورد تداخل RNA است.
در حالی که دانشمندان با سرعت هر چه بیشتر به سمت آزمایشهای بالینی پیش میروند، روی توسعه یک تکنیک جدید و امیدوارانه بهبود یافته تداخل RNA نیز کار میکنند. برای توضیح تفاوتها با تکنیکهای موجود، باید کمی در مورد نحوه خوانده شدن ژنها برای ساخت پروتئینها توضیح دهیم. با ما همراه باشید – ارزشش را دارد!
DNA و RNA چیستند؟
DNA طرح اولیه ساخت انسان است. این یک مولکول طولانی است که از قطعات به هم چسبیده به نام بازها تشکیل شده است که در 4 ‘طعم’ مختلف وجود دارند – C A G و T. اینها حروفی هستند که کد ژنتیکی ما با آنها نوشته شده است.
‘مارپیچ دوگانه’ DNA از دو رشته تشکیل شده است که در کنار هم قرار میگیرند. هر رشته یک رشته از بازها است و دو رشته توسط پیوندهای شیمیایی بین بازهای روی رشتههای مقابل به هم متصل میشوند. A با T جفت میشود و C با G جفت میشود.
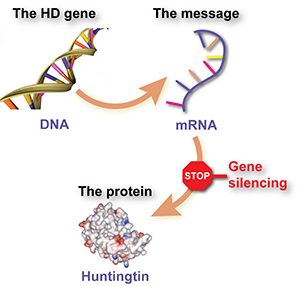
برای رسیدن از DNA به یک پروتئین، باید یک ‘نسخه کاری’ از DNA ساخته شود. این نسخه ‘پیامرسان’ RNA یا mRNA نامیده میشود. RNA ارتباط نزدیکی با DNA دارد اما کمی متفاوت به نظر میرسد.
mRNA قالبی است که به سلول میگوید چگونه یک پروتئین را کنار هم قرار دهد. هر زمان که یک سلول هر پروتئینی – از جمله پروتئین هانتینگتین – را میسازد، این کار را با خواندن دستورالعملهای موجود در mRNA مربوط به آن پروتئین انجام میدهد.
مداخله در mRNA هانتینگتین – یا ‘هدف قرار دادن پیامرسان’ – از کنار هم قرار گرفتن پروتئین هانتینگتین جلوگیری میکند و اساس خاموشسازی ژن در تداخل RNA است.
بسیار خب – برگردیم به خاموشسازی ژن
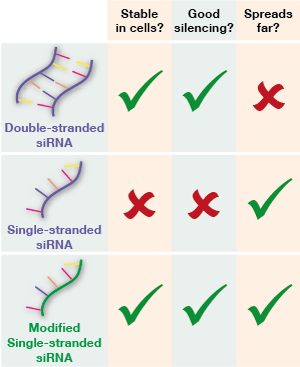
تا کنون، تکنیکهای خاموشسازی ژن مبتنی بر RNA از مولکولهای RNA دورشتهای به نام siRNA استفاده کردهاند. RNA دورشتهای تا به حال مورد نیاز بود، زیرا RNA تکرشتهای قبل از اینکه بتواند خاموشسازی را انجام دهد، توسط مکانیسمهای پاکسازی زباله خود سلولها از بین میرود.
RNA دورشتهای پس از ورود به سلولها، باید به رشتههای تکی جدا شود تا به مولکول پیام mRNA هانتینگتین متصل شود. سپس یک آنزیم در سلولها mRNA را میجود، به طوری که پروتئین جهشیافته هرگز ساخته نمیشود.
ما میدانیم که این روش انجام کار میتواند به طور چشمگیری میزان پروتئین HD جهشیافته ساخته شده در سلولها را کاهش دهد. چیزی که کمتر در مورد آن مطمئن هستیم این است که آیا رشته ناخواستهای که جدا میشود، عوارض جانبی بدی روی سلولها دارد یا خیر. این احتمال وجود دارد که بدن حملهای را به رشته باقیمانده آغاز کند و باعث آسیب شود. احتمال دیگر این است که رشته باقیمانده به mRNA دیگری متصل شود و از ساخت پروتئینهای مهم دیگر جلوگیری کند.
مولکولهای siRNA دورشتهای در مغز خیلی دور پخش نمیشوند و درمان مناطق بزرگ مغز را دشوار میکنند.
یک مشکل نهایی siRNAهای دورشتهای این است که برای اینکه به بافتهای مناسب برسند و کار خود را انجام دهند، باید به روشی پیچیده بستهبندی شوند.
مطالعاتی در مدلهای حیوانی موش و میمون مبتلا به بیماری هانتینگتون انجام شده است که نشان میدهد siRNAها ایمن و مؤثر هستند، اما دانشمندان گروه محتاطی هستند زیرا باید قبل از ارائه هر گونه درمان به انسانهای ارزشمند، واقعاً در مورد ایمنی مطمئن باشیم. آخرین کاری که میخواهیم انجام دهیم این است که HD را بدتر کنیم.
siRNA تکرشتهای
یک ایده برای کاهش خطر اثرات بد تداخل RNA، تولید یک siRNA تکرشتهای است. اما چگونه میتوانیم بر مشکل پایداری غلبه کنیم – آن عادت آزاردهنده سلولها در خرد کردن داروی RNA تکرشتهای؟
پس از تلاشهای فراوان، گروهی از محققان به سرپرستی دیوید کوری در دالاس، با همکاری شرکت داروسازی ISIS، به تازگی اعلام کردهاند که بالاخره آن را حل کردهاند. برای اینکه تصوری از هیجانی که این موضوع ایجاد کرده است به شما بدهیم، این موضوع در نه یک، بلکه دو مقاله ‘پشت سر هم’ در همان نسخه از مجله برتر Cell اعلام شد. چه موفقیتی!
تیم کوری با ایجاد برخی تغییرات شیمیایی در تلاشهای قبلی، یک siRNA تکرشتهای ساختهاند و توانستند آن را در یک محلول آب نمک ساده بستهبندی کنند. آنها با موفقیت siRNA تکرشتهای را به فضاهای مایع اطراف مغز در یک مدل موش مبتلا به HD تزریق کردند و توانستند نشان دهند که به mRNA هانتینگتین متصل میشود و از ساخت پروتئین HD جلوگیری میکند.
برد-برد-برد؟
علاوه بر این، برخلاف داروهای siRNA دورشتهای که قبلاً آزمایش شدهاند، اثرات siRNA تکرشتهای به جای اینکه محدود به ناحیه کوچکی در نزدیکی تزریق باشد، در سراسر مغز پخش میشود. حداقل در این موشها، siRNA تکرشتهای یک برد-برد ایجاد کرد: پایدار بود و بیشتر پخش میشد.
آنها با این موضوع قانع نشدند و کار را فراتر بردند. با کمی تغییر در ساختار مولکول خود، توانستند یک siRNA تکرشتهای نیز ایجاد کنند که فقط تولید پروتئین HD جهشیافته را مسدود میکرد و از ساخت نسخه طبیعی پروتئین HD جلوگیری نمیکرد. آنها این کار را با هدف قرار دادن siRNA به کشش ‘CAG’ غیرطبیعی طولانی در ژن HD انجام دادند.
با یک siRNA تکرشتهای، نیازی نیست نگران این باشیم که رشته دوم چه کاری ممکن است انجام دهد، و با هدف قرار دادن فقط mRNA هانتینگتین جهشیافته، نگرانی کمتری در مورد اثرات احتمالی توقف تولید پروتئین HD طبیعی وجود دارد.
بعدش چی؟
بنابراین این روش جدید در مدلهای موش ایمن و مؤثر به نظر میرسد. اکنون باید قبل از اینکه حتی به فکر ورود به آزمایشهای انسانی باشیم، مطمئن شویم که در مدلهای حیوانی بزرگتر دیگر نیز ایمن و مؤثر است. این اتفاق اکنون در حال رخ دادن است!
سوالات باقی مانده
قبل از اینکه تداخل RNA تکرشتهای بتواند در افراد آزمایش شود، باید به چند سوال پاسخ داده شود.
اول، برخی ژنهای دیگر با یک کشش CAG در آنها وجود دارد. ما هنوز نمیدانیم که آیا معرفی siRNAهای تکرشتهای که این کششهای CAG را هدف قرار میدهند، ممکن است ناخواسته ژنهای مهم دیگر را خاموش کند یا خیر.
دوم، مشکل تحویل. چگونه میخواهیم به قسمتهای مهم مغز بیماران مبتلا به بیماری هانتینگتون برسیم؟ خوشبختانه، محققان در HD و سایر بیماریها در حال حاضر روی این موضوع کار میکنند. یک آزمایش داروی مشابه ساخته شده از DNA تکرشتهای در حال حاضر در بیماری نورون حرکتی (ALS) در حال آزمایش است.
در نهایت، چگونه میخواهیم اثربخشی درمان را اندازهگیری و نظارت کنیم؟ در مدلهای حیوانی، میتوانیم این کار را با نگاه کردن به بافت مغز و اندازهگیری میزان پروتئین هانتینگتین ساخته شده انجام دهیم. انجام این کار در انسانها بسیار دشوارتر است، اما دانشمندان برتر روی آن کار میکنند و ما فکر میکنیم آماده شروع آزمایشها در بیماران مبتلا به بیماری هانتینگتون هستیم.
کاربردهای بالقوه بیشتر برای siRNA تکرشتهای
یک پیش نمایش نهایی از یک کاربرد احتمالی دیگر siRNA تکرشتهای. محققان همچنین در حال بررسی استفاده از آن در ترکیب با تحقیقات سلولهای بنیادی هستند. اساساً، آنها در حال کار بر روی گرفتن سلولهای پوست از افراد مبتلا به بیماری هانتینگتون و تبدیل آن سلولهای پوست به نورونها هستند. سپس میتوان آن نورونها را با siRNAهای تکرشتهای درمان کرد تا سطح پروتئین HD مضر قبل از پیوند مجدد آنها به مغز کاهش یابد.
سالها طول خواهد کشید تا ترکیب siRNA تکرشتهای با سلولهای بنیادی مشتق شده از بیمار به عنوان یک درمان مورد استفاده قرار گیرد، اما این یک ایده جالب است و خوب است بدانیم که همه راهها در حال بررسی هستند. در همین حال، انتظار داریم siRNA تکرشتهای به سرعت به سمت آزمایشهای بالینی پیشرفت کند.
بیشتر بدانید
برای اطلاعات بیشتر در مورد سیاست افشای اطلاعات ما، به سوالات متداول مراجعه کنید…


